565/AB XXI.GP
B e a n t w o r t u n g
der Anfrage der Abgeordneten Petrovic, Freundinnen und
Freunde betreffend illegale Praktiken bei Futter - und Tierarzneimitteln
Nr. 537/J
Zur gegenständlichen Anfrage führe ich Folgendes aus:
Zu Frage 1:
Gemäß § 24 Abs.3 des Tierärztegesetzes darf der Tierarzt im Rahmen von ständi -
gen Betreuungsverhältnissen entgegen dem Vorbehalt des § 12 den Tierhalter in die
Anwendung von Arzneimitteln bei landwirtschaftlichen Nutztieren einbinden. Dabei
ist die für die betreffende Arzneispezialität vorgeschriebene Art der Lagerung einzu -
halten. Gemäß § 12 Abs.1 des Tierärztegesetzes dürfen Impfungen, Injektionen,
Transfusionen, instillationen und Blutabnahmen bei Tieren nur von Tierärzten aus -
geübt werden. Angebrochene Injektionsflaschen sind ausnahmslos im Kühlschrank
zu lagern.
Zu Frage 2:
Die in der Anfrage genannten Arzneimittelspezialitäten sind durchwegs verschrei -
bungspflichtig. Im übrigen verweise ich auf meine Ausführungen zu Frage 1
Zu Frage 3:
Wechselwirkungen werden, soweit sie bekannt sind, in der Fachinformation zu jeder
zugelassenen Arzneispezialität angeführt. Die gleichzeitige Verabreichung verschie -
dener Medikamente ist im allgemeinen nicht üblich.
Zu Frage 4:
Bei den angeführten Medikamenten sind hinsichtlich der Fleischqualität folgende
Wartezeiten zu beachten:
BAYTRIL 5 % - Durchstichflasche für Tiere; essbare Gewebe (Rind, Schwein)
10 Tage, Milch 4 Tage.
Monzal - Durchstichflasche für Tiere; essbare Gewebe und Milch je 1 Tag
Stresnil - Durchstichflasche
für Schweine; essbare Gewebe 5 Tage
Suacron - Durchstichflasche für Tiere; essbare Gewebe Schwein 3 Tage, Rind
1 Tag, Milch 1 Tag
Synpitan - vet - Durchstichflasche für Tiere; keine Wartezeit erforderlich
Im Falle der Nichteinhaltung der vorgeschriebenen Wartezeit ist eine Überschreitung
der Rückstandshöchstwerte zu erwarten. Rückstandsbelastetes Fleisch ist als ge -
sundheitsschädlich zu bewerten.
Zu den Fragen 5, 7 und 9:
Alle angeführten Medikamente sind in Österreich zugelassen. Die Bezeichnung der
Produkte „Baytril“ und "Monzal" ist jedoch für die in Deutschland vermarkteten Wa -
ren gebräuchlich.
Nicht der österreichischen Zulassung und Aufmachung entsprechende Medikamente
(auch nicht, wenn identische Mittel im Inland zugelassen sind) dürfen nicht in Ver -
kehr gebracht oder angewendet werden, sofern nicht eine Bewilligung gemäß Arz -
neiwareneinfuhrgesetz erteilt wurde.
Die Kontrollmöglichkeiten an den österreichischen Grenzen sind durch die Öffnung
der Grenzen (EWR - Binnenmarkt) und durch die Zunahme des grenzüberschreiten -
den Reiseverkehrs zurückgegangen. Wird anlässlich von Rückstandsuntersuchun -
gen eine Überschreitung der zulässigen Rückstandshöchstwerte festgestellt, werden
vom zuständigen Amtstierarzt Erhebungen über die Ursache durchgeführt. Gegen
illegale Importe von Arzneimitteln wird im Rahmen der gesetzlichen Möglichkeiten
vorgegangen.
Zu Frage 6:
Es ist unklar, welcher Betrieb in der Anfrage gemeint ist. Daten über Betreuungsver -
hältnisse zwischen landwirtschaftlichen Betrieben und Tierärzten liegen meinem
Ressort nicht vor. Solche Betreuungsverhältnisse sind im Rahmen von Tiergesund -
heitsdiensten üblich, die in einigen Bundesländern eingerichtet sind. Für die Überprü -
fung der in § 24 Abs. 3 Tierärztegesetz beschriebenen Vorgangsweise sind die Be -
zirksverwaltungsbehörden zuständig.
Zu Frage 8:
Am Futterzusatzoffsektor sind EU - weit (und damit auch in Österreich) nur noch 4
Antibiotika (Monensin - Na, Salinomycin - Na, Flavophospholipol und Avilamycin) als
Leistungs - bzw. Wachstumsförderer zugelassen.
Daneben sind allerdings eine ganze Reihe von Zusatzstoffen als Coccidiostatica und
andere Arzneimittel, darunter jedoch nicht Tetracycline, autorisiert. Diese Gruppe ist
strengen Zulassungskriterien und demgemäßen Bestimmungen, die die Herstellung
solcher Stoffe betrifft (Zulassung der Betriebe), unterworfen.
Die Futtermittelprüfung wird routinemäßig vom Bundesamt und Forschungszentrum
für Landwirtschaft, Institut für Futtermittel bzw. vom Bundesamt für Agrarbiologie in
Linz durchgeführt. Nach dortiger Mitteilung wurden im Jahre 1999 1900 Proben ge -
zogen. Damit liegt Österreich im oberen
Drittel der EU - Mitgliedsstaaten.
Die Schwierigkeit, bislang nicht auffällige Kontaminationen (wie z.B. Dioxin), wenn
sie überhaupt oder in erhöhtem Ausmaß auftreten, zu erfassen, liegt in der Fäche -
rung des analytischen Screenings, das heißt es können möglicherweise schwierig zu
detektierende Substanzen nicht durch allgemeine Prüfverfahren erkannt werden.
Das wesentliche überhöhte Auftreten von Dioxin wurde in Deutschland auch nur
durch ein routinemäßiges Monitoring der Milch und in Belgien durch manifeste Effek -
te (bis zum Tod) bei den Tieren (Hühner, Kücken), denen kontaminiertes Tierfutter
verabreicht wurde, entdeckt.
Dessen ungeachtet sind eine Verbesserung des Kontrollsystems und gezielte
Suchmethoden sowie ein Frühwarnsystem ähnlich wie bei den Lebensmitteln erfor -
derlich, wie es die Europäische Kommission in ihrem jüngsten Weißbuch beabsich -
tigt.
Die Häufigkeit und die Anzahl der Probenahmen ist durch die vorhandene Laborka -
pazität vorgegeben, wobei die jährlich von der EU - Kommission zu genehmigenden
Rückstandskontrollpläne stets eingehalten werden.
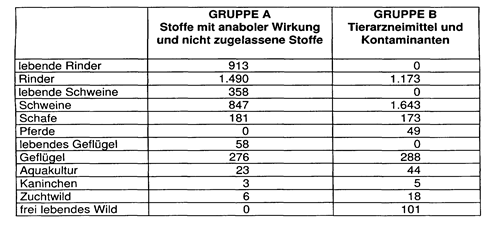
Im Kalenderjahr 1998 wurde folgende Anzahl von Lebendtier - und Fleischproben
gezogen und auf nachstehende Rückstands - bzw. Stoffarten untersucht:
 |
Die Kompetenz für die Probeziehung und Kontrolle im Futtermittelbetrieb liegt beim
Bundesminister für Land - und Forstwirtschaft, Umwelt und Wasserwirtschaft.