10968/J XXVII. GP
Eingelangt am 13.05.2022
Dieser Text wurde elektronisch übermittelt. Abweichungen vom Original sind
möglich.
Anfrage
der Abgeordneten Fiona Fiedler, Kolleginnen und Kollegen
an den Bundesminister für Soziales‚ Gesundheit‚ Pflege und Konsumentenschutz
betreffend Erstattungskodex der Sozialversicherungen
Der Erstattungskodex der Sozialversicherungen gibt einen Überblick, für welche Medikamente die Sozialversicherungen die Kosten übernehmen. Jährlich wird aber nur ein Überblick veröffentlicht, allerdings entspricht der Datenzeitraum dabei immer von Dezember bis November und ermöglicht damit keinem Kalenderüberblick um bisherige Datenreihen zu vervollständigen.
Der Prozess, der zur Aufnahme eines Medikaments in den Erstattungskodex führt, ist reglementiert, allerdings muss ein Pharmaproduzent immer erst einen Antrag um Aufnahme in den EKO stellen, damit dies erfolgen kann - der EKO muss also auch für Produzenten ein attraktives Abgeltungsmodell darstellen, um Österreich zu einem wirtschaftlich interessanten Markt zu machen. Ohne dies ist langfristig keine Versorgungssicherheit gegeben, da Produkte andernfalls bevorzugt in anderen Ländern angeboten werden oder einfach nicht von Versicherungsträgern abgedeckt werden können.
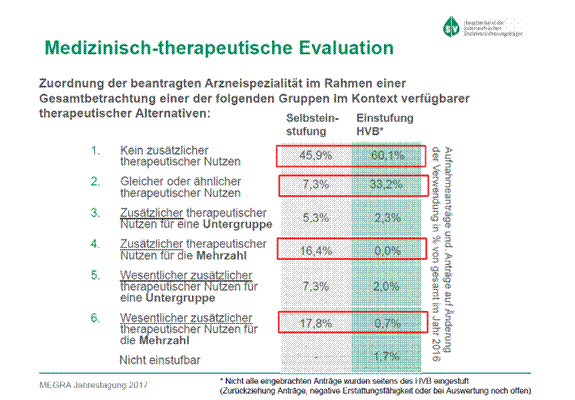
Auch bei abgedeckten Arzneimitteln stellt sich aber immer wieder die Frage, welchen Nutzen die Regelungen des EKO in den Vordergrund stellen. So gibt es häufig unterschiedliche Einschätzungen von Patientennutzen und divergierende Ansichten der Industrie und der HEK, welche neuen Produkte einen höheren Nutzen erfüllen und welche für eine Neuzulassung eine Preisreduktion anzubieten zu haben. Dies zeigt sich auch an den unterschiedlichen Angaben zur Medizinisch-therapeutischen Evaluation, bei denen die HEK den neuen Nutzen für Patienten oft geringer einschätzt, als Produzenten dies selbst tun. Das ist zwar ein erwartbares Ergebnis, allerdings wird nicht mit erklärt, wie die Heilmittel-Evaluierungskommission zu ihren Einschätzungen kommt.
Kürzliche Änderungen des Allgemeinen Sozialversicherungsgesetzes verlangen jetzt aber auch bei neuen Markteintritten ohne Erstattungsschema, dass die österreichischen Marktpreise unter dem europäischen Durchschnittspreis liegen müssen. Welche Auswirkungen das langfristig auf die Versorgungssicherheit haben wird, muss sich erst zeigen. Dennoch stellen sich zwischenzeitlich Fragen, wie sich die Zahlen der Aufnahmen in den Erstattungskodex entwickelt haben - besonders, da in früheren Anfragen noch nicht unbedingt finale Zahlen gemeldet wurde.
Die unterfertigten Abgeordneten stellen daher folgende
Anfrage:
Bitte um Aufschlüsselung aller Antworten nach Originalpräparat, Generikum, Biologika und Biosimilar, Angabe des Innovationsgrades nach Einschätzung des Antragstellers sowie des Dachverbandes und einzelnen Jahren
- Wie viele Anträge um Aufnahme in den Erstattungskodex wurden seit 2019 gestellt?
- Wie viele dieser Anträge bezogen sich auf Nachfolgeprodukte im Sinne einer gleichen oder sehr ähnlichen Indikation bisher erstatteter Arzneimittel?
i. Für wie viele dieser Mittel wurden die Anträge genehmigt?(Bitte um Angabe, bei wie vielen der Preis im Vergleich zum Vergleichsprodukt nach oben/ unten/ gar nicht geändert wurde)
ii. Für wie viele dieser Mittel wurden die Anträge abgelehnt?
- Wie viele Anträge um Aufnahme in den Erstattungskodex wurden seit 2019 genehmigt?
- Wie viele Anträge um Aufnahme in den Erstattungskodex wurden seit 2019 abgelehnt? (Bitte um Angabe der Gründe der Ablehnung zusätzlich zu den oben erbetenen Kategorien)
- Wie viele Anträge um Aufnahme in den Erstattungskodex wurden seit 2019 zurückgezogen?
- Wie viele Anträge um Änderung der Verwendung im Gelben und im Grünen Bereich des Erstattungskodex wurden seit 2019 gestellt? (Bitte um Angabe der Änderungskategorie (Verwendung, Packungsgröße und Preiserhöhung) für alle nachfolgenden Fragen zu Punkt 2
- Wie viele dieser Anträge bezogen sich auf Nachfolgeprodukte im Sinne einer gleichen oder sehr ähnlichen Indikation bisher erstatteter Arzneimittel?
i. Für wie viele dieser Mittel wurden die Anträge genehmigt? (Bitte Angabe, bei wie vielen der Preis im Vergleich zum Vorgängerprodukt nach oben/ unten/ gar nicht geändert wurde zusätzlich zu den oben erbetenen Kategorien)
ii. Für wie viele dieser Mittel wurden die Anträge abgelehnt?
- Wie viele dieser Anträge bezogen sich auf Änderungen nach Innovationsgrad 4 (neue Darreichungsform)?
i. Wie viele der Anträge auf Änderungen nach Innovationsgrad 4 wurden mit einer Preissenkung zum bisherigen Produkt genehmigt und wie hoch war die durchschnittliche Preissenkung?
- Wie viele Anträge um Änderung im Erstattungskodex wurden seit 2019 genehmigt?
i. Wie viele dieser Anträge bezogen sich auf Änderungen nach Innovationsgrad 4 (neue Darreichungsform)?
ii. Wie viele der Anträge auf Änderungen nach Innovationsgrad 4 wurden mit einer Preissenkung zum bisherigen Produkt genehmigt?
- Wieviele viele Anträge um Änderung im Erstattungskodex führten zu einer Überführung vom Gelben in den Grünen Bereich?
- Wie viele Anträge um Änderung im Erstattungskodex wurden seit 2019 abgelehnt?
- Wie viele Produkte konnten nach einer Änderung der Verwendung zum selben Preis im EKO verbleiben?
- Wie viele
- Wie viele Anträge um Streichung aus dem Erstattungskodex wurden seit 2019 gestellt?
- Wie viele Anträge um Streichung aus dem Erstattungskodex wurden seit 2019 genehmigt?
- Wie viele Anträge um Streichung aus dem Erstattungskodex wurden seit 2019 zurückgezogen?
- Wie viele Verfahren auf Änderung wurden seitens des Hauptverbandes eingeleitet?
- Wie viele Verfahren auf Änderung, die seitens des Hauptverbandes eingeleitet wurden, wurden mit einer Einigung abgeschlossen? (Bitte um Aufschlüsselung nach Originalpräparat, Generikum, Biologika und Biosimilar inklusive Angabe der jeweiligen ATC Kategorie nach Jahren sowie Inhalt der Einigung wie beispielsweise Änderung der Verschreibbarkeit)
- Wie viele viele Anträge um Änderung im Erstattungskodex führten zu einer Überführung vom Gelben in den Grünen Bereich?
- Wie viele Verfahren auf Änderung, die seitens des Hauptverbandes eingeleitet wurden, führten zu einer Streichung?
- Wie viele Verfahren auf Streichung wurden seitens des Hauptverbandes eingeleitet? (Bitte um Angaben der Gründe wie beispielsweise Nichtlieferfähigkeit für alle nachfolgenden Fragen zu Punkt 5)
- Wie viele Verfahren auf Streichung, die seitens des Hauptverbandes eingeleitet wurden, wurden mit einer Einigung abgeschlossen?
- Wie viele Verfahren auf Änderung, die seitens des Hauptverbandes eingeleitet wurden, wurden mit einer Einigung auf eine Preissenkung abgeschlossen?
- Wie hoch war im Durchschnitt die Preissenkung?
- Wie viele Verfahren auf Streichung, die seitens des Hauptverbandes eingeleitet wurden, führten zu einer Streichung?